Effect of shading on saponin content and biochemical indexes of Paris polyphylla Smith var. chinensis (Franch.) Hara in northern Zhejiang
-
摘要: 七叶一枝花[Paris polyphylla Smith var. chinensis (Franch.) Hara]为药材重楼的药源植物, 具有较好的抗肿瘤、抗炎等作用; 野生七叶一枝花生于海拔1800~3200 m林下, 目前已资源匮乏, 人工栽培尚不成规模, 同时, 七叶一枝花生长受光强影响显著, 强度不适时植株易萎蔫死亡, 因此, 研究遮阴处理对人工培育优质七叶一枝花具有重要意义。本文以6年生的七叶一枝花为试验材料, 设置不同遮阴条件(70%、80%、90%), 对重楼皂苷含量、光合色素含量、抗氧化酶活性、MDA含量、可溶性物质含量等指标进行测定, 探究遮阴程度对七叶一枝花中皂苷成分的影响规律。结果显示, 重楼皂苷含量与SOD活性、POD活性、MDA含量存在显著负相关性(P<0.05), 与叶绿素a/b、CAT活性、可溶性蛋白质含量存在显著正相关(P<0.05); 在遮阴80%的处理下, 重楼皂苷含量最高(重楼皂苷Ⅰ为1.45 mg∙g−1, 重楼皂苷Ⅵ为2.52 mg∙g−1, 重楼皂苷Ⅶ为3.22 mg∙g−1, 总重楼皂苷为7.19 mg∙g−1); 同时该遮阴下各项光合色素指标和可溶性蛋白质含量(11.28 mg∙g−1)均为最高, POD (2.89 U∙g−1∙min−1)和SOD (105.01 U∙g−1∙min−1)活性最低, MDA (11.90 μmol∙g−1)和脯氨酸(FP, 8.88 mg∙g−1)含量最低。综上所述, 不同的遮阴程度对七叶一枝花中重楼皂苷含量和初生代谢影响较大; 其中80%遮阴处理有利于其重楼皂苷合成和积累, 有利于光合色素和可溶性蛋白质含量的提高; 较高或较低遮阴对七叶一枝花生长和重楼皂苷的含量均产生不利影响。本研究结果可为优化七叶一枝花人工栽培措施及获得优质药材提供理论参考。Abstract: Paris polyphylla Smith var. chinensis (Franch.) Hara is a rare traditional herb, the rhizome of which (named Paridis Rhizoma) is commonly used for its antitumor and anti-inflammatory effects. P. polyphylla mainly comprises saponins, the production of which is affected by the intensity of light. Therefore, the determination of the most suitable shading degree for this herb plant in northern Zhejiang can lay the foundation for the promotion of its’ artificial cultivation. In this study, the effects of different degrees of shading on the accumulation of saponins in P. polyphylla and on changes in their biochemical indices were explored. The plants were maintained at the arboretum test site of Zhejiang Agriculture and Foresty University, China (30°15ʹN, 119°43ʹE) from June to September 2019. Black shading nets were used to create different shading conditions (70%, 80%, and 90%). Six-year-old P. polyphylla plants were used as the test materials, and their contents of saponins, photosynthetic pigments, malondialdehyde (MDA), and osmotic adjustment substances as well as antioxidative enzymes activities were measured to determine their response to shading conditions.The results showed that the saponin content was negatively correlated with the superoxide dismutase (SOD) activity, peroxidase (POD) activity, and MDA content (P<0.01), but positively correlated with the chlorophyll a/b ratio, catalase (CAT) activity, and soluble protein content (P<0.05). The 80% shading condition was most beneficial to saponin accumulation, as evidenced by the highest total saponin content (7.19 mg·g−1) in the plant compared with that yielded by the 70% (3.79 mg·g−1) and 90% (1.85 mg·g−1) shading conditions. The contents of all types of saponins were the highest under the 80% shading condition (polyphyllin Ⅰ: 1.45 mg·g−1; polyphyllin Ⅵ: 2.52 mg·g−1; and polyphyllin Ⅶ: 3.22 mg·g−1). Additionally, the contents of photosynthetic pigments (total chlorophyll: 4.72 mg·g−1) and soluble proteins (11.28 mg·g−1) were higher in plants under 80% shading than in those under 70% (total chlorophyll: 2.94 mg·g−1; soluble protein: 9.23 mg·g−1) and 90% shading (total chlorophyll: 3.81 mg·g−1; soluble protein: 7.72 mg·g−1). However, the activities of POD (2.89 U·g−1·min−1) and SOD (105.01 U·g−1·min−1), contents of MDA (11.90 μmol·g−1) and proline (8.88 mg·g−1) in plants under 80% shading were lower than those in plants under 70% (POD: 3.20 U·g−1·min−1; SOD: 123.38 U·g−1·min−1; and MDA: 13.89 μmol∙g−1; proline: 11.48 mg·g−1) and 90% shading (POD: 4.90 U·g−1·min−1; SOD: 165.09 U·g−1·min−1; and MDA: 15.46 μmol∙g−1; proline: 12.68 mg·g−1). Moreover, compared with the plants treated with 80% shading, those treated with 70% and 90% shading showed significantly lower contents of total saponins. In summary, different degrees of shading significantly influenced the P. polyphylla saponin content and primary metabolism. The data from this study provide a theoretical reference for the artificial cultivation and quality improvement of P. polyphylla in northern Zhejiang.
-
七叶一枝花[Paris polyphylla Smith var. chinensis (Franch.) Hara]为百合科(Liliaceae)重楼属药用植物, 又名重楼、蚤休、灯台七等, 收录在《中华人民共和国药典》[1]中, 与云南重楼[P. polyphylla Smith var. yunnanensis (Franch.) Hand.-Mazz.]共同列为药材重楼的基源植物, 以地下根茎入药, 具有清热解毒、消肿止痛等药效, 可用于惊风抽搐、蛇虫咬伤等症, 是云南白药、宫血宁、季德胜蛇药片等多种中成药的重要原料之一[2]; 其入药部位含有多种甾体皂苷, 具有抗肿瘤、抗心肌缺血、止血等药理作用[3]。七叶一枝花分布于我国浙江[4]、云南、四川、湖南等地, 原生在海拔1800~3200 m林下; 近年来, 由于价格攀升, 野生七叶一枝花资源逐渐稀少, 急需提升人工种植技术缓解医药需求压力。
在七叶一枝花生长发育过程中, 适宜的光照是必不可少的条件之一。事实上, 光照是影响植物生长发育的重要环境因子, 光强能够影响光合色素含量, 改变叶绿体结构和光合速率[5-6], 对可溶性物质含量产生显著影响; 并且, 适宜的光强可以提高某些次生代谢物质的含量[7]。当植物遭受光强胁迫时, 其生理生化进程随之发生改变, 产生大量活性氧, 引起保护酶系统反应[8-9], 直接或间接促进某些次生代谢产物生成。例如, 贾兵等[10]研究表明, 外源过氧化氢可以提高三七[Panax notoginseng (Burkill) F. H. Chen ex C. Chow & W. G. Huang]皂苷含量; 同时, 保护酶活性增加, 清除过多氧化产物带来的毒性。影响皂苷类化合物合成的因素很多, 光照也是影响皂苷合成的重要环境因子之一, 光反应产物是皂苷类合成过程中的必需物质[11], 在适宜光强范围内, 皂苷含量随处理时间增加而提高, 超过范围后, 则随之下降[12]。郑顺林等[13]研究表明, 光强可影响七叶一枝花的光合特性, 在四川地区, 40%和60%左右遮光度下光合效率较高, 遮光度大于80%会造成弱光胁迫; 梁娟等[14]研究发现, 光强能够影响湖南地区七叶一枝花的重楼皂苷含量, 以70%遮阴度含量最高。以上研究表明, 光强是影响七叶一枝花光合特性、重楼皂苷含量的关键生态因子; 同时, 因地域差异, 七叶一枝花对遮阴程度的要求不同, 且重楼皂苷的积累存在差异。但是在以往研究中与重楼皂苷积累可能有关的生理指标并未同步检测, 同时浙北地区七叶一枝花研究尚较少。
本文基于“光照是否调控七叶一枝花重楼皂苷积累”的问题思考, 以6年生七叶一枝花为试验材料, 研究了不同遮阴条件对其重楼皂苷含量变化的影响, 同时明晰抗逆保护酶活性指标、可溶性渗透调节物质含量指标、光合色素含量指标的变化规律, 从而筛选适宜浙北地区七叶一枝花生长和皂苷含量提高的光照条件, 为实现七叶一枝花大面积林下仿生种植或大田人工栽培提供参考, 为光调控提升药材品质提供理论依据。
1. 材料与方法
1.1 试验材料与试验地点概况
供试材料采自浙江农林大学(浙江临安, 30°15′30″N, 119°43′27″E)植物园, 地处浙江省西北部, 属亚热带季风气候, 温暖湿润, 光照充足, 雨量充沛, 四季分明; 全年降雨量约1600 mm, 无霜期年平均为237 d, 年平均气温16.4 ℃。试验材料采用田间试验方式, 种植于透气、透水性良好的砂质壤土, 经浙江农林大学植物学科夏国华博士鉴定为百合科重楼属植物七叶一枝花。
1.2 试验方法
试验材料分别栽培于以下3种遮阴梯度环境下: 70%、80%和90%, 利用调整遮阳网层数和剪洞法控制遮阴程度。透气遮阳棚高约2 m, 下边缘距离地面0.2 m, 使试验苗不受早晚阳光直射; 使用照度计(胜利电子仪器有限公司, 中国杭州)于晴天正午12:00定期监测, 确保遮阴度准确。七叶一枝花的株行距0.5 m×0.5 m, 每种植穴种植1株。处理时间为2019年6—9月; 3种遮阴梯度温度条件、水肥管理一致。
1.3 测定指标及方法
1.3.1 重楼皂苷含量测定
试验结束时, 每个处理选取长势基本一致的试验苗3株, 整株挖取七叶一枝花试验苗, 去除地上部分、杂质、泥土, 洗净, 冻干, 制备样品粉末, 过50目筛, 备用。
采用高效液相色谱法(HPLC)测定重楼皂含量。测定指标和条件参照中华人民共和国药典(2015版)[1], 计算线性回归方程; 同时根据药典要求, 进行方法学考察, 包括精密度试验、稳定性试验、重复性试验及加样回收试验, 并计算相关相对标准偏差(RSD)值。
色谱柱: 天津万象恒远科技有限公司C18色谱柱(4.6 mm × 250 mm, 5 μm), 以乙腈为流动相A, 水为流动相B进行梯度洗脱(0~40 min, 30%~60% A, 70%~40% B; 40~50 min, 60%~30% A, 40%~70% B)。流速为0.8 mL·min−1, 进样量10 μL, 检测波长为203 nm, 柱温30 ℃。
1.3.2 生理生化指标测定
试验结束时, 每个处理随机采集长势相近似、健康无虫害的七叶一枝花新鲜叶片, 每个处理设5次生物学重复, 根据李合生[15]方法测定以下指标: 采用乙醇浸提法测定叶绿素a (chla)、叶绿素b (chlb)和类胡萝卜素(Car)含量(mg∙g−1), 采用愈创木酚法测定过氧化物酶(POD)活性(U∙g−1∙min−1), 采用氮蓝四唑光还原法测定超氧化物歧化酶(SOD)活性(U∙g−1∙min−1),采用紫外吸收法测定过氧化氢酶(CAT)活性(U∙g−1∙min−1), 采用硫代巴比妥酸比色法测定丙二醛(MDA)含量(μmol∙g−1), 采用磺基水杨酸法测定脯氨酸(FP)含量(mg∙g−1), 采用考马斯亮蓝法测定可溶性蛋白质(SP)含量(mg∙g−1), 采用茚三酮法测定游离氨基酸(FAA)含量(mg∙g−1)。可溶性糖(SS)含量(mg∙g−1)测定采用蒽酮法[16]。
1.4 数据分析
利用Origin 2018和SPSS 22.0软件进行数据处理及统计分析, 结果以“平均值±标准差”表示。
2. 结果与分析
2.1 遮阴处理对七叶一枝花重楼皂苷含量的影响
2.1.1 线性回归关系结果
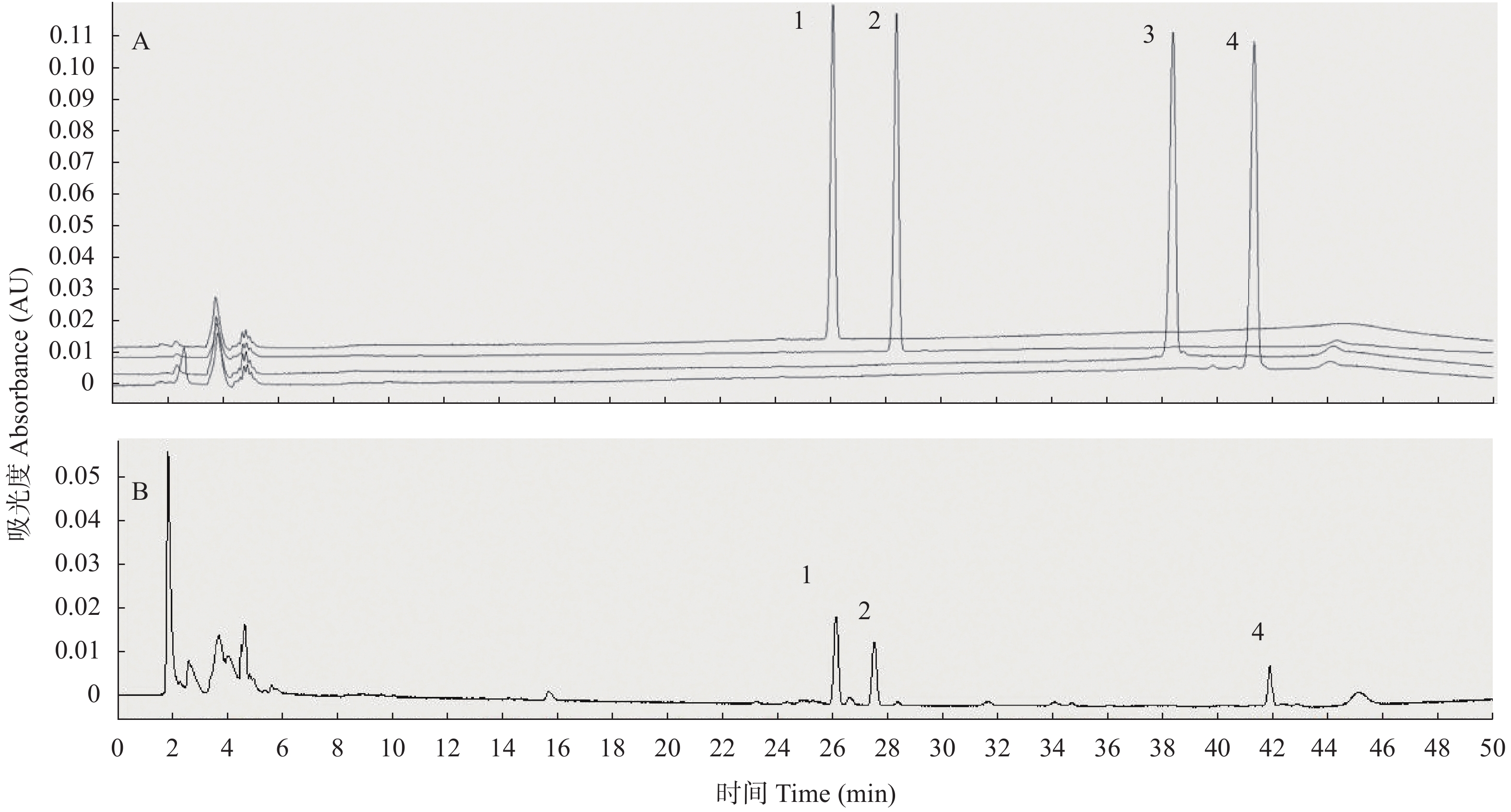
重楼皂苷Ⅰ、重楼皂苷Ⅱ、重楼皂苷Ⅵ、重楼皂苷Ⅶ标准品和样品的HPLC图谱见图1。根据标准品的出峰图(图1A)计算线性回归方程(表1), r值均大于0.999, 线性关系良好; 将各样品峰面积带入方程, 计算样品含量。
表 1 重楼皂苷标准品溶液线性回归方程Table 1. HPLC regression equation of reference solution of four authentic saponins皂苷类型 Saponins type 回归方程 Regression equation r 线性范围 Linear range (μg) 重楼皂苷Ⅰ Polyphyllin Ⅰ y=418 655x−26 726 0.9991 0.0398~3.9844 重楼皂苷Ⅱ Polyphyllin Ⅱ y=345 133x−14 445 0.9994 0.0398~3.9884 重楼皂苷Ⅵ Polyphyllin Ⅵ y=487 983x−22 655 0.9995 0.0399~3.994 重楼皂苷Ⅶ Polyphyllin Ⅶ y=318 393x−13 975 0.9991 0.0399~3.9956 2.1.2 方法学考察结果
方法学考察结果显示该测定条件稳定且良好: 精密度考察试验计算得RSD范围为0.27%~2.56%, 表明仪器精密度良好; 稳定性考察试验计算得RSD范围为0.81%~0.95%, 表明样品溶液在16 h内检测对结果无影响, 稳定性良好; 重复性试验计算峰面积RSD范围为1.44%~2.97%, 表明该方法重现性良好; 加样回收试验计算得回收率在95.49%~98.17%, 计算峰面积RSD范围为0.14%~2.62%, 表明回收情况良好。
2.1.3 样品测定结果
对各遮阴处理下七叶一枝花根茎进行重楼皂苷含量测定, 并根据回归方程计算结果。如表2所示, 在80%遮阴处理条件下, 重楼皂苷Ⅰ、重楼皂苷Ⅵ和重楼皂苷Ⅶ均最高; 且含量总和仍为最高(7.19 mg∙g−1), 分别比70%和90%处理的重楼皂苷含量高89.71%和284.49%, 该结果符合2015版药典[1]规定(重楼皂苷Ⅰ、重楼皂苷Ⅱ、重楼皂苷Ⅵ和重楼皂苷Ⅶ总量在0.6%以上); 但是未达到现行2020版药典[17]的规定(重楼皂苷Ⅰ、重楼皂苷Ⅱ和重楼皂苷Ⅶ总量在0.6%以上)。3种处理中, 重楼皂苷Ⅵ和重楼皂苷Ⅶ含量、皂苷总含量表现出显著性差异, 而重楼皂苷Ⅰ含量差异并不显著。此外, 在本试验所有处理样品中均未检出重楼皂苷Ⅱ。
表 2 不同程度遮阴对七叶一枝花根茎中重楼皂苷含量的影响Table 2. Saponins contents of Paris polyphylla Smith var. chinensis (Franch.) Hara under different shading treatmentsmg∙g−1 遮阴度
Shading degree (%)重楼皂苷Ⅰ
Polyphyllin Ⅰ重楼皂苷Ⅱ
Polyphyllin Ⅱ重楼皂苷Ⅵ
Polyphyllin Ⅵ重楼皂苷Ⅶ
PolyphyllinⅦ重楼皂苷含量
Saponins content70 1.06±0.21a — 1.25±0.40b 1.48±0.24b 3.79±0.54b 80 1.45±0.28a — 2.52±0.09a 3.22±0.11a 7.19±0.42a 90 1.11±0.01a — 0.23±0.06c 0.53±0.07c 1.87±0.13c 同列不同小写字母表示不同遮阴度间在P<0.05水平差异显著。Different lowercase letters in the same column indicate significant differences at P<0.05 level among treatments. 2.2 遮阴处理对七叶一枝花抗氧化酶活性及氧化产物含量的影响
2.2.1 遮阴处理对抗氧化酶活性的影响
不同遮阴处理七叶一枝花抗氧化酶活性结果如表3所示, SOD和POD活性变化趋势一致, 均以遮阴80%处理最低, 分别为105.00 U∙g−1∙min−1和2.89 U∙g−1∙min−1; 遮阴度为90%时, SOD和POD活性急剧上升(165.09 U∙g−1∙min−1、4.90 U∙g−1∙min−1), 增幅分别为57.23% (P<0.05)和69.55% (P<0.05)。CAT活性随遮阴度上升而逐渐下降, 以70%处理最高, 为21.43 U∙g−1∙min−1, 遮阴度为90%时, CAT活性显著低于其他处理, 为5.74 U∙g−1∙min−1。以上结果表明, 与其他处理相比, 80%遮阴处理下的七叶一枝花受到光胁迫较小, 而70%和90%处理下七叶一枝花的保护酶系统响应更强烈, 同时, 90%处理下七叶一枝花对于过氧化氢的清除能力低于70%处理。CAT位于活性氧清除系统的下游, 将SOD和POD分解活性氧时产生的过氧化氢转化为无害的水和氧, 90%处理后的SOD和POD活性最高、CAT活性最低, 表明其生理状态并不乐观, 无法将植物体内的有害物质完全分解掉; 70%和80%处理则相反, 表明其生理状态好于90%处理。
表 3 不同遮阴处理下七叶一枝花的抗氧化酶活性变化Table 3. Antioxidative enzymes activities of Paris polyphylla Smith var. chinensis (Franch.) Hara under different shading treatmentsU·g−1·min−1 遮阴度
Shading degree (%)SOD活性
SOD activityPOD活性
POD activityCAT活性
CAT activity70 123.38±4.99b 3.20±0.06b 21.43±1.01a 80 105.00±3.67c 2.89±0.15c 19.78±1.85a 90 165.09±10.94a 4.90±0.09a 5.74±0.97b 同列不同小写字母表示不同遮阴度间在P<0.05水平差异显著。Different lowercase letters in the same column indicate significant differences at P<0.05 level among different treatments. 2.2.2 遮阴处理对MDA积累的影响
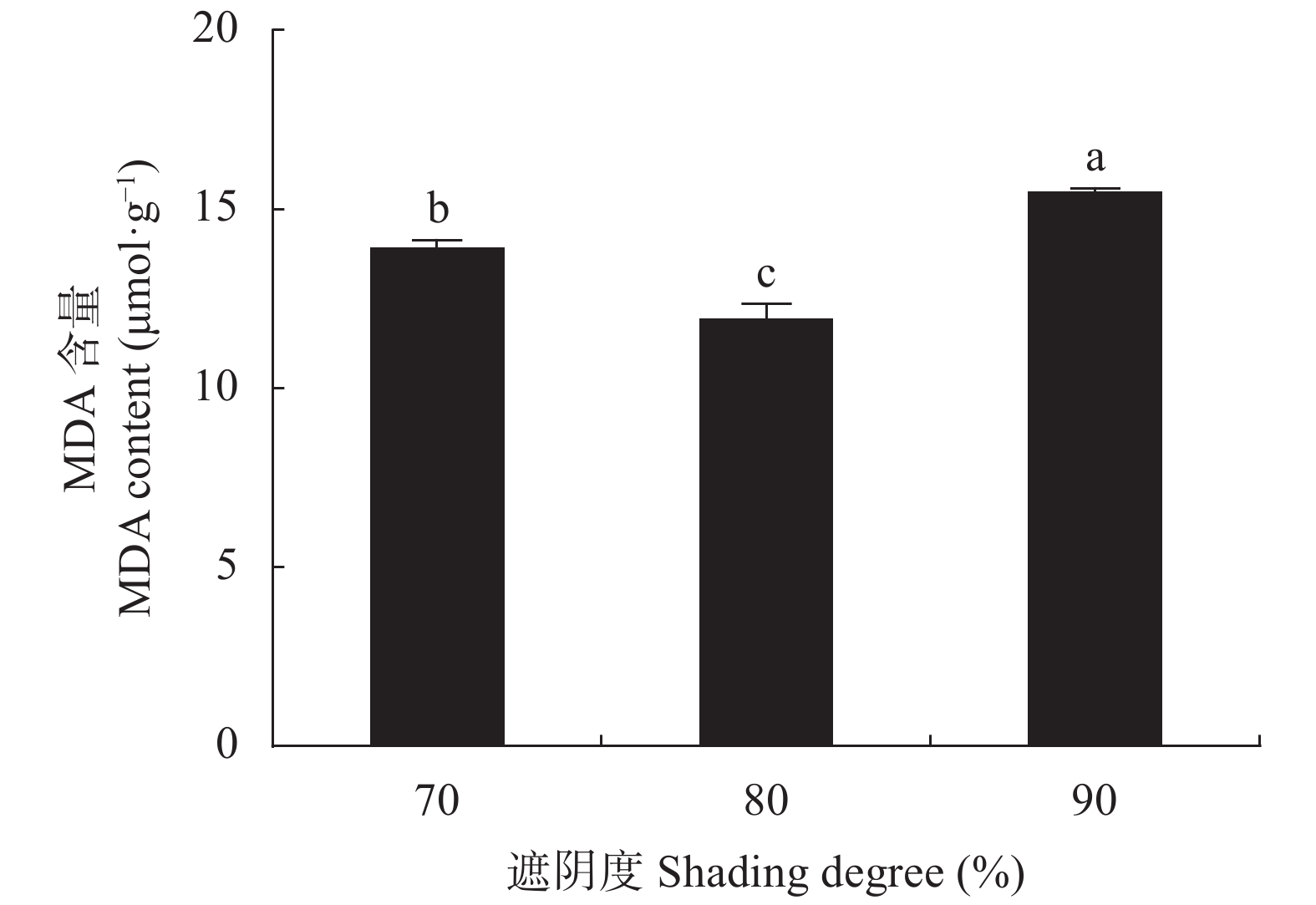
氧化产物MDA含量随遮阴度的变化而变化(图2), 其中, 以80%遮阴处理下含量最低, 为11.90 μmol∙g−1, 较数值最高的90%处理(15.46 μmol∙g−1)低23.03% (P<0.05)。该结果进一步佐证, 80%遮阴环境下七叶一枝花膜脂过氧化程度更低, 遭受的逆境伤害较小, 而90%遮阴已对七叶一枝花产生弱光胁迫, 遭受损伤较大。结合MDA含量和保护酶活性分析认为, 90%遮阴不利于七叶一枝花的生存, 80%遮阴对七叶一枝花的生存是有利的, 70%遮阴仅次于80%遮阴。
2.3 遮阴处理对七叶一枝花光合色素含量的影响
由表4可以看出, 遮阴70%处理叶绿素a、b, 类胡萝卜素含量, 叶绿素a/b以及叶绿素总量均为最低, 80%遮阴处理显著提高了光合色素含量, 较70%遮阴处理, 叶绿素a、叶绿素b、类胡萝卜素含量、叶绿素a/b和叶绿素总量分别提高70.83%、30.38%、85.85%、32.72%和60.54%, 差异均达显著水平(P<0.05), 并且80%和90%遮阴处理的叶绿素a、叶绿素b和叶绿素总量显著高于70%处理。说明80%遮阴能够促进光合色素的合成, 并且遮阴程度的提升能够提高叶绿素a和叶绿素b含量。
表 4 不同遮阴条件下七叶一枝花的光合色素含量变化Table 4. Photosynthetic pigment contents of Paris polyphylla Smith var. chinensis (Franch.) Hara under different shading遮阴度
Shading degree (%)叶绿素a
Chlorophyll a
(mg∙g−1)叶绿素b
Chlorophyll b
(mg∙g−1)类胡萝卜素
Carotinoid
(mg∙g−1)叶绿素a/b
Chlorophyll a/b叶绿素总量
Total chlorophyll
(mg∙g−1)70 2.16±0.09c 0.79±0.03b 8.48±0.34b 2.72±0.02b 2.94±0.11c 80 3.69±0.25a 1.03±0.04a 15.76±1.31a 3.61±0.42a 4.72±0.21a 90 2.86±0.06b 0.95±0.01a 10.15±0.16b 3.00±0.04b 3.81±0.07b 同列不同小写字母表示不同遮阴度间在P<0.05水平差异显著。Different lowercase letters in the same column indicate significant differences at P<0.05 level among different treatments. 2.4 遮阴处理对七叶一枝花可溶性物质含量的影响
各处理之间可溶性物质的含量存在显著差异, 并且随着遮阴程度的增加, 可溶性糖、可溶性蛋白质、游离氨基酸和脯氨酸含量变化不同。如表5所示, 与90%遮阴处理相比, 70%和80%遮阴处理的可溶性糖含量增幅分别为246.43% (P<0.05)和207.14% (P<0.05), 说明随着遮阴程度的升高, 可溶性糖含量逐渐下降。各处理的可溶性蛋白质含量随遮阴度变化呈先上升后下降的趋势, 且差异显著, 其中, 80%处理可溶性蛋白质含量最高, 为11.28 mg∙g−1, 较90%处理提高46.11% (P<0.05)。游离氨基酸含量随着遮阴度上升而显著增加, 90%处理下游离氨基酸含量最高, 为7.54 mg∙g−1, 较70%处理增加56.11% (P<0.05)。脯氨酸含量随遮阴度变化呈先下降后上升趋势, 80%处理下脯氨酸含量最低, 为8.88 mg∙g−1, 较70%处理和90%处理分别降低22.64%和29.97% (P<0.05)。
表 5 不同遮阴处理下七叶一株花的可溶性物质含量变化Table 5. Soluble substances contents of Paris polyphylla Smith var. chinensis (Franch.) Hara under different shading treatmentsmg∙g−1 遮阴度 Shading degree (%) 可溶性糖 Soluble sugar 可溶性蛋白质 Soluble protein 游离氨基酸 Free amino acid 脯氨酸 Proline 70 0.97±0.01a 9.23±0.01b 4.83±0.02c 11.48±0.22a 80 0.86±0.01b 11.28±0.05a 5.53±0.23b 8.88±0.47b 90 0.28±0.01c 7.72±0.04c 7.54±0.61a 12.68±0.26a 同列不同小写字母表示不同遮阴度间在P<0.05水平差异显著。Different lowercase letters in the same column indicate significant differences at P<0.05 level among different treatments. 由此可见, 七叶一枝花的初生代谢是复杂的内在联系, 光强对其影响不是简单、线性的, 但仍然存在一定规律, 综合分析以上数据认为, 80%遮阴处理有利于七叶一枝花生长。
2.5 七叶一枝花重楼皂苷含量与生化指标的相关性分析
重楼皂苷含量与生化指标的相关性分析如表6所示, 其含量与SOD活性、POD活性、MDA含量之间存在极显著的负相关性, 相关系数分别为−0.90、−0.89和−0.95; 与CAT活性存在显著正相关性, 相关系数为0.79。本结果说明在一定光强范围内, 当SOD活性和POD活性越低、MDA含量越低、CAT活性越高时, 七叶一枝花中重楼皂苷的含量越高, 即适宜的光照强度或较小的光照胁迫, 有利于重楼皂苷含量的提升。
表 6 七叶一枝花重楼皂苷含量及各生化指标的相关性分析Table 6. Correlation analysis of polyphyllin content with biochemical indexes of Paris polyphylla Smith var. chinensis (Franch.)重楼皂苷
PolyphyllinSOD CAT POD MDA 叶绿素a
Chlorophyll
a叶绿素b
Chlorophyll
b叶绿素a/b
Chlorophyll
a/b叶绿素总量
Total
chlorophyll类胡萝卜素
Carotinoid可溶性糖
Soluble sugar可溶性蛋白质
Soluble protein游离氨基酸
Free amino acid脯氨酸
Proline重楼皂苷
Polyphyllin1.00 −0.90** 0.79* −0.89** −0.95** 0.46 −0.15 0.70* −0.02 −0.25 0.50 0.99** 0.03 −0.29 SOD −0.90** 1.00 −0.90** 0.95** 0.90** −0.33 0.33 −0.45 0.18 0.50 −0.69* −0.91** 0.22 0.59 CAT 0.79* −0.90** 1.00 −0.95** −0.74* 0.20 −0.59 0.50 −0.42 −0.54 0.89** 0.79* −0.54 −0.65 POD −0.89** 0.95** −0.95** 1.00 0.88** −0.28 0.37 −0.59 0.18 0.41 −0.81** −0.89** 0.38 0.66 MDA −0.95** 0.90** −0.74* 0.88** 1.00 −0.48 −0.03 −0.63 −0.16 0.13 −0.44 −0.97** −0.09 0.31 叶绿素a
Chlorophyll a0.46 −0.33 0.20 −0.28 −0.48 1.00 0.32 0.64 0.39 0.02 −0.08 0.50 0.40 0.21 叶绿素b
Chlorophyll b−0.15 0.33 −0.59 0.37 −0.03 0.32 1.00 0.09 0.96** 0.74* −0.72* −0.12 0.79* 0.53 叶绿素a/b
Chlorophyll a/b0.70* −0.45 0.50 −0.59 −0.63 0.64 0.09 1.00 0.25 0.16 0.33 0.67* 0.03 −0.02 叶绿素总量
Total chlorophyll−0.02 0.18 −0.42 0.18 −0.16 0.39 0.96** 0.25 1.00 0.66 −0.53 0.01 0.66 0.37 类胡萝卜素
Carotinoid−0.25 0.50 −0.54 0.41 0.13 0.02 0.74* 0.16 0.66 1.00 −0.52 −0.28 0.46 0.46 可溶性糖
Soluble sugar0.50 −0.69* 0.89** −0.81** −0.44 −0.08 −0.72* 0.33 −0.53 −0.52 1.00 0.47 −0.85** −0.87** 可溶性蛋白质
Soluble protein0.99** −0.91** 0.79* −0.89** −0.97** 0.50 −0.12 0.67* 0.01 −0.28 0.47 1.00 0.06 −0.27 游离氨基酸
Free amino acid0.03 0.22 −0.54 0.38 −0.09 0.40 0.79* 0.03 0.66 0.46 −0.85** 0.06 1.00 0.78* 脯氨酸 Proline −0.29 0.59 −0.65 0.66 0.31 0.21 0.53 −0.02 0.37 0.46 −0.87** −0.27 0.78* 1.00 **: P<0.01; *: P<0.05. 此外, 重楼皂苷含量与可溶性蛋白质含量存在极显著正相关, 相关系数为0.99; 与叶绿素a/b存在显著正相关, 相关系数为0.70, 与其他光合色素和可溶性物质含量间无显著相关性, 说明在代谢过程中, 可溶性蛋白质含量和叶绿素a/b的比值越高, 重楼皂苷含量有可能越高。
3. 讨论
七叶一枝花在我国分布范围较广, 但是由于其生长缓慢、易休眠、难繁殖、且产量低, 无法满足医药需求, 致使无序采挖, 其野生资源日渐濒危。人工种植可缓解七叶一枝花资源匮乏的现状, 不过, 我国幅员辽阔, 不同产地光照条件差异明显, 采取的遮阴度也不尽相同。例如, 梁娟等[14]研究表明, 在湖南地区, 七叶一枝花在遮光70%条件下光合速率、皂苷含量最高, 遮阴程度过高或过低不利于七叶一枝花的光合作用和皂苷积累; 郑顺林等[13]在四川省宝兴县地区开展研究, 发现七叶一枝花在遮光40%或60%条件下光合速率最高, 并提出遮阴在40%~60%范围内, 有利于提高七叶一枝花的光饱和点、降低光补偿点和干物质的积累。本文结果表明, 80%的遮阴处理, 可使七叶一枝花根茎中重楼皂苷含量最高; 结合各项生化指标, 说明在浙北地区的夏季, 该遮阴条件有利于七叶一枝花有效成分合成。其次, 与80%遮阳相比, 70%和90%遮阴处理对皂苷类化合物积累不利。匡双便等[18]研究结果表明, 三七总皂苷在8.4%透光条件下最高, 并且极显著高于2.9%透光条件, 22.0%和11.0%透光条件结果仅次于8.4%处理, 且彼此间相差不大, 而1.1%透光率下生物量和总皂苷含量均最低, 可以推测, 三七总皂苷的积累需要至少8.4%的光照强度。这提示我们, 七叶一枝花中重楼皂苷的积累需要适宜的光照。此外, 本研究中并未测得重楼皂苷Ⅱ, 可能与七叶一枝花的产地有关[19], 相关原因和机理有待进一步研究解析。
在重楼皂苷的合成途径中, 糖类化合物广泛存在并参与其中, 如前体物质薯蓣皂苷元经糖苷化合成重楼皂苷Ⅰ和重楼皂苷Ⅱ, 经羟化、糖苷化合成重楼皂苷Ⅵ和重楼皂苷Ⅶ[20]。在本研究中, 可溶性糖含量以70%处理最高, 与Li等[21]对鱼腥草(Houttuynia cordata Thunb.)和郭品湘等[22]对木番茄(Solanum wrightii Benth.)的研究相近, 即可溶性糖含量会随着光照强度的下降而降低, 这可能与植物光合效率有关, 遮阴降低了植物的光合效率, 减少了光合产物的积累。
但是, 次生代谢是一个极复杂的过程, 单一的可溶性糖含量变化不足以直接影响重楼皂苷的积累。苏文华等[23]和Kouki等[24]的研究结果指出, 一定程度的胁迫可使植物生长减慢, 促使物质合成更多地流向次生代谢, 并且影响次生代谢物种类。本文中, 重楼皂苷含量与SOD活性、POD活性、MDA含量之间存在极显著的负相关, 表明在适宜的光照条件下, 七叶一枝花会合成和积累较多的皂苷类物质。70%处理后的CAT活性、MDA和脯氨酸含量也较高, 说明该遮阴条件对于七叶一枝花会造成一定程度强光胁迫, 刺激POD和SOD活性增加, 进而有助于将超氧阴离子转化为过氧化氢; 同时, 较高的CAT活性有助于过氧化氢的分解, 间接促进可溶性糖的合成与积累。而90%遮阴条件下POD和SOD活性最高、CAT活性最低, 表明该条件下七叶一枝花不能够及时清除细胞内产生的过氧化氢, 导致了MDA的大量积累, 结合重楼皂苷测定结果, 说明90%遮阴对七叶一枝花伤害更强, 并且不利于皂苷的积累。
重楼皂苷与可溶性蛋白质含量存在显著正相关, 而可溶性蛋白质包含着参与光合作用各反应阶段的大量酶[25], 其含量高, 有利于植物在遮荫下维持光合作用, 为次生代谢提供必要的前体物质。例如孙克香等[26]研究表明, 强光胁迫下可溶性蛋白质含量较高的甜椒(Capsicum fructescens L.)幼苗具有更低的MDA含量, 与本研究中可溶性蛋白质含量以遮阴80%时最高的结果相似。
重楼皂苷与其他可溶性物质相关性不大, 但是可溶性物质既是植物的光合产物, 又是重要的渗透调节物质, 能够提高细胞保水能力, 保证细胞的正常生理功能。其中, 脯氨酸含量与植物所处光环境有关, 在逆境时其含量上升, 通过增加细胞渗透势, 对植物起到保护作用, 并进一步维持细胞膜的结构。例如, 黄河腾等[27]研究指出, 当光照条件相对于木奶果(Baccaurea ramiflora Lour.)幼苗而言偏高或偏低时, 脯氨酸含量会增加, 与本研究结果是相同的。此外, 游离氨基酸含量以90%遮阴处理后最高, 应与光强过低有关。吴能表等[28]研究结果表明, 较高的遮阴条件可导致长春花[Catharanthus roseus (L.) G. Don]叶片的碳同化率降低, 继而引起氨基酸同化速率降低, 进一步导致游离氨基酸的积累。结合SOD、POD活性和MDA、脯氨酸含量均最高, 90%遮阴已引起七叶一枝花抗氧化系统的响应, 即该条件对七叶一枝花造成了弱光胁迫。陶巧静等[29]发现西洋杜鹃(Rhododendron hybridum Ker Gawl.)在弱光胁迫条件下, 叶片超微结构发生变化, 细胞结构存在破损缺失, 可溶性蛋白质含量降低。据此分析, 本文90%遮阴处理下游离氨基酸含量较高、可溶性蛋白质含量较低可能与细胞结构破坏、蛋白质降解有关。
重楼皂苷与叶绿素a/b存在显著正相关。七叶一枝花光合色素的含量和比例变化与光照强度有关, 在适宜遮阴条件(80%)显著高于其他处理, 与王宇等[7]在黄芪(Astragalus membranaceus Bunge.)的结果相似, 即光合作用随着光照强度的增加先增强后减弱, 而叶绿素含量随着遮阴程度增加呈先升高后降低的趋势。分析认为, 这与植物光反应中心的结构有关, 过低或过高的光照强度都会损伤植物的叶绿体类囊体结构[30-31], 降低气孔导度, 抑制光合作用, 尤其是高光强会加剧植物光氧化现象, 引起叶片失绿, 使叶绿素含量降低[32-33]。
4. 结论
本研究结果表明, 适宜的遮阴度有助于提高七叶一枝花重楼皂苷的含量, 提高光合色素含量, 降低过氧化物含量, 过低或过高的遮阴程度均会产生不利影响。综合各项指标得出本文结论, 80%的遮阴度较适合浙北地区七叶一枝花的人工种植。同时, 结合前人研究结果可知, 在生产中应注意因地制宜、因时制宜, 结合本地条件, 选择适宜七叶一枝花生长和重楼皂苷合成的遮光梯度, 进一步满足医药需求。
-
表 1 重楼皂苷标准品溶液线性回归方程
Table 1 HPLC regression equation of reference solution of four authentic saponins
皂苷类型 Saponins type 回归方程 Regression equation r 线性范围 Linear range (μg) 重楼皂苷Ⅰ Polyphyllin Ⅰ y=418 655x−26 726 0.9991 0.0398~3.9844 重楼皂苷Ⅱ Polyphyllin Ⅱ y=345 133x−14 445 0.9994 0.0398~3.9884 重楼皂苷Ⅵ Polyphyllin Ⅵ y=487 983x−22 655 0.9995 0.0399~3.994 重楼皂苷Ⅶ Polyphyllin Ⅶ y=318 393x−13 975 0.9991 0.0399~3.9956 表 2 不同程度遮阴对七叶一枝花根茎中重楼皂苷含量的影响
Table 2 Saponins contents of Paris polyphylla Smith var. chinensis (Franch.) Hara under different shading treatments
mg∙g−1 遮阴度
Shading degree (%)重楼皂苷Ⅰ
Polyphyllin Ⅰ重楼皂苷Ⅱ
Polyphyllin Ⅱ重楼皂苷Ⅵ
Polyphyllin Ⅵ重楼皂苷Ⅶ
PolyphyllinⅦ重楼皂苷含量
Saponins content70 1.06±0.21a — 1.25±0.40b 1.48±0.24b 3.79±0.54b 80 1.45±0.28a — 2.52±0.09a 3.22±0.11a 7.19±0.42a 90 1.11±0.01a — 0.23±0.06c 0.53±0.07c 1.87±0.13c 同列不同小写字母表示不同遮阴度间在P<0.05水平差异显著。Different lowercase letters in the same column indicate significant differences at P<0.05 level among treatments. 表 3 不同遮阴处理下七叶一枝花的抗氧化酶活性变化
Table 3 Antioxidative enzymes activities of Paris polyphylla Smith var. chinensis (Franch.) Hara under different shading treatments
U·g−1·min−1 遮阴度
Shading degree (%)SOD活性
SOD activityPOD活性
POD activityCAT活性
CAT activity70 123.38±4.99b 3.20±0.06b 21.43±1.01a 80 105.00±3.67c 2.89±0.15c 19.78±1.85a 90 165.09±10.94a 4.90±0.09a 5.74±0.97b 同列不同小写字母表示不同遮阴度间在P<0.05水平差异显著。Different lowercase letters in the same column indicate significant differences at P<0.05 level among different treatments. 表 4 不同遮阴条件下七叶一枝花的光合色素含量变化
Table 4 Photosynthetic pigment contents of Paris polyphylla Smith var. chinensis (Franch.) Hara under different shading
遮阴度
Shading degree (%)叶绿素a
Chlorophyll a
(mg∙g−1)叶绿素b
Chlorophyll b
(mg∙g−1)类胡萝卜素
Carotinoid
(mg∙g−1)叶绿素a/b
Chlorophyll a/b叶绿素总量
Total chlorophyll
(mg∙g−1)70 2.16±0.09c 0.79±0.03b 8.48±0.34b 2.72±0.02b 2.94±0.11c 80 3.69±0.25a 1.03±0.04a 15.76±1.31a 3.61±0.42a 4.72±0.21a 90 2.86±0.06b 0.95±0.01a 10.15±0.16b 3.00±0.04b 3.81±0.07b 同列不同小写字母表示不同遮阴度间在P<0.05水平差异显著。Different lowercase letters in the same column indicate significant differences at P<0.05 level among different treatments. 表 5 不同遮阴处理下七叶一株花的可溶性物质含量变化
Table 5 Soluble substances contents of Paris polyphylla Smith var. chinensis (Franch.) Hara under different shading treatments
mg∙g−1 遮阴度 Shading degree (%) 可溶性糖 Soluble sugar 可溶性蛋白质 Soluble protein 游离氨基酸 Free amino acid 脯氨酸 Proline 70 0.97±0.01a 9.23±0.01b 4.83±0.02c 11.48±0.22a 80 0.86±0.01b 11.28±0.05a 5.53±0.23b 8.88±0.47b 90 0.28±0.01c 7.72±0.04c 7.54±0.61a 12.68±0.26a 同列不同小写字母表示不同遮阴度间在P<0.05水平差异显著。Different lowercase letters in the same column indicate significant differences at P<0.05 level among different treatments. 表 6 七叶一枝花重楼皂苷含量及各生化指标的相关性分析
Table 6 Correlation analysis of polyphyllin content with biochemical indexes of Paris polyphylla Smith var. chinensis (Franch.)
重楼皂苷
PolyphyllinSOD CAT POD MDA 叶绿素a
Chlorophyll
a叶绿素b
Chlorophyll
b叶绿素a/b
Chlorophyll
a/b叶绿素总量
Total
chlorophyll类胡萝卜素
Carotinoid可溶性糖
Soluble sugar可溶性蛋白质
Soluble protein游离氨基酸
Free amino acid脯氨酸
Proline重楼皂苷
Polyphyllin1.00 −0.90** 0.79* −0.89** −0.95** 0.46 −0.15 0.70* −0.02 −0.25 0.50 0.99** 0.03 −0.29 SOD −0.90** 1.00 −0.90** 0.95** 0.90** −0.33 0.33 −0.45 0.18 0.50 −0.69* −0.91** 0.22 0.59 CAT 0.79* −0.90** 1.00 −0.95** −0.74* 0.20 −0.59 0.50 −0.42 −0.54 0.89** 0.79* −0.54 −0.65 POD −0.89** 0.95** −0.95** 1.00 0.88** −0.28 0.37 −0.59 0.18 0.41 −0.81** −0.89** 0.38 0.66 MDA −0.95** 0.90** −0.74* 0.88** 1.00 −0.48 −0.03 −0.63 −0.16 0.13 −0.44 −0.97** −0.09 0.31 叶绿素a
Chlorophyll a0.46 −0.33 0.20 −0.28 −0.48 1.00 0.32 0.64 0.39 0.02 −0.08 0.50 0.40 0.21 叶绿素b
Chlorophyll b−0.15 0.33 −0.59 0.37 −0.03 0.32 1.00 0.09 0.96** 0.74* −0.72* −0.12 0.79* 0.53 叶绿素a/b
Chlorophyll a/b0.70* −0.45 0.50 −0.59 −0.63 0.64 0.09 1.00 0.25 0.16 0.33 0.67* 0.03 −0.02 叶绿素总量
Total chlorophyll−0.02 0.18 −0.42 0.18 −0.16 0.39 0.96** 0.25 1.00 0.66 −0.53 0.01 0.66 0.37 类胡萝卜素
Carotinoid−0.25 0.50 −0.54 0.41 0.13 0.02 0.74* 0.16 0.66 1.00 −0.52 −0.28 0.46 0.46 可溶性糖
Soluble sugar0.50 −0.69* 0.89** −0.81** −0.44 −0.08 −0.72* 0.33 −0.53 −0.52 1.00 0.47 −0.85** −0.87** 可溶性蛋白质
Soluble protein0.99** −0.91** 0.79* −0.89** −0.97** 0.50 −0.12 0.67* 0.01 −0.28 0.47 1.00 0.06 −0.27 游离氨基酸
Free amino acid0.03 0.22 −0.54 0.38 −0.09 0.40 0.79* 0.03 0.66 0.46 −0.85** 0.06 1.00 0.78* 脯氨酸 Proline −0.29 0.59 −0.65 0.66 0.31 0.21 0.53 −0.02 0.37 0.46 −0.87** −0.27 0.78* 1.00 **: P<0.01; *: P<0.05. -
[1] 国家药典委员会. 中华人民共和国药典[S]. 一部. 北京: 中国医药科技出版社, 2015: 260 Chinese Pharmacopoeia Commission. Pharmacopoeia of the People’s Republic of China[S]. Beijing: China Medical Science Press, 2015: 260
[2] 丁立帅, 赵猛, 李燕敏, 等. 七叶一枝花根茎和地上部分提取物镇痛抗炎作用研究[J]. 天然产物研究与开发, 2018, 30(5): 832−839 DING L S, ZHAO M, LI Y M, et al. Study on the anti-nociceptive and anti-inflammatory effects of the extract of aerial part and rhizome of Paris polyphylla var. chinensis[J]. Natural Product Research and Development, 2018, 30(5): 832−839
[3] 杨远贵, 张霁, 张金渝, 等. 重楼属植物化学成分及药理活性研究进展[J]. 中草药, 2016, 47(18): 3301−3323 doi: 10.7501/j.issn.0253-2670.2016.18.027 YANG Y G, ZHANG J, ZHANG J Y, et al. Research progress in chemical constituents in plants of Paris L. and their pharmacological effects[J]. Chinese Traditional and Herbal Drugs, 2016, 47(18): 3301−3323 doi: 10.7501/j.issn.0253-2670.2016.18.027
[4] 闫道良, 田风光, 段承俐, 等. 浙江省七叶一枝花种质资源现状与表型多元统计分析[J]. 浙江林业科技, 2015, 35(3): 6−10 YAN D L, TIAN F G, DUAN C L, et al. Investigation and phenotypic analysis on germplasm resources of Paris polyphylla var. chinensis in Zhejiang[J]. Journal of Zhejiang Forestry Science and Technology, 2015, 35(3): 6−10
[5] 王璐, 李艳丽, 熊欢, 等. 温度胁迫对锥栗幼苗叶片结构及光合特性的影响[J]. 江西农业大学学报, 2020, 42(4): 692−699 WANG L, LI Y L, XIONG H, et al. Effect of temperature stress on leaf structure and photosynthesis of chinquapin (Castanea henryi)[J]. Acta Agriculturae Universitatis Jiangxiensis, 2020, 42(4): 692−699
[6] 张辉, 王荷, 张蓓蓓, 等. 光强对黑麦草萌发生长、叶片叶绿素含量及光系统Ⅱ的影响[J]. 干旱地区农业研究, 2018, 36(4): 207−213 doi: 10.7606/j.issn.1000-7601.2018.04.30 ZHANG H, WANG H, ZHANG B B, et al. Effects of light intensity on germination, growth, chlorophyll content and photosystem Ⅱ of leaves in ryegrass (Lolium perenne L.)[J]. Agricultural Research in the Arid Areas, 2018, 36(4): 207−213 doi: 10.7606/j.issn.1000-7601.2018.04.30
[7] 王宇, 刘洋, 刘佳, 等. 不同光照强度对黄芪主要次生代谢物含量的影响[J]. 应用与环境生物学报, 2017, 23(5): 928−933 WANG Y, LIU Y, LIU J, et al. Effect of light intensity on the contents of main secondary metabolites in Astragalus[J]. Chinese Journal of Applied and Environmental Biology, 2017, 23(5): 928−933
[8] 杨培芳, 史红专, 郭巧生, 等. 光照强度对紫花地丁物质和能量代谢的影响[J]. 中国中药杂志, 2020, 45(24): 5944−5950 YANG P F, SHI H Z, GUO Q S, et al. Effects of light intensity on material and energy metabolism of Viola yedoensis[J]. China Journal of Chinese Materia Medica, 2020, 45(24): 5944−5950
[9] ZUSHI K, SUEHARA C, SHIRAI M. Effect of light intensity and wavelengths on ascorbic acid content and the antioxidant system in tomato fruit grown in vitro[J]. Scientia Horticulturae, 2020, 274: 109673 doi: 10.1016/j.scienta.2020.109673
[10] 贾兵, 范伟, 陈庚, 等. 建立UPLC-MS联合HPLC方法探究外源物质对三七叶皂苷含量和生长的影响[J]. 云南农业大学学报: 自然科学版, 2019, 34(1): 116−123 JIA B, FAN W, CHEN G, et al. Development of UPLC-MS combined with HPLC technique to explore the effects of exogenous substances on the saponin contents and growth of Panax notoginseng leaves[J]. Journal of Yunnan Agricultural University: Natural Science, 2019, 34(1): 116−123
[11] 焦晓林, 高微微. 环境因子对药用植物三萜皂苷合成影响的研究进展[J]. 中草药, 2011, 42(2): 398−402 JIAO X L, GAO W W. Advances in studies on influence of environmental factors on triterpenoid saponin synthesis in medicinal plants[J]. Chinese Traditional and Herbal Drugs, 2011, 42(2): 398−402
[12] 曾燕, 郭兰萍, 杨光, 等. 环境生态因子对药用植物皂苷成分的影响[J]. 中国实验方剂学杂志, 2012, 18(17): 313−318 doi: 10.3969/j.issn.1005-9903.2012.17.089 ZENG Y, GUO L P, YANG G, et al. Effect of environmental ecological factors on saponins of medicinal plant[J]. Chinese Journal of Experimental Traditional Medical Formulae, 2012, 18(17): 313−318 doi: 10.3969/j.issn.1005-9903.2012.17.089
[13] 郑顺林, 田孟良, 刘金亮, 等. 人工驯化栽培中弱光胁迫对七叶一枝花光合特性的影响[J]. 中药材, 2014, 37(9): 1518−1522 ZHENG S L, TIAN M L, LIU J L, et al. Effects of Low-light stress on photosynthetic characteristics of Paris polyphylla var. chinensis in artificial domestication cultivation[J]. Journal of Chinese Medicinal Materials, 2014, 37(9): 1518−1522
[14] 梁娟, 易涛, 叶漪. 遮阴对七叶一枝花光合特性及皂苷含量的影响[J]. 江苏农业科学, 2016, 44(4): 265−267 LIANG J, YI T, YE Y. Effects of shading on photosynthetic characteristics and saponin contents of Paris polyphylla[J]. Jiangsu Agricultural Sciences, 2016, 44(4): 265−267
[15] 李合生. 植物生理生化实验原理和技术[M]. 北京: 高等教育出版社, 2000: 134, 258–260, 184 LI H S. Principles and Techniques of Plant Physiological Biochemical Experiment[M]. Beijing: Higher Education Press, 2000: 134, 258–260, 184
[16] 位杰, 吴翠云, 蒋媛, 等. 蒽酮法测定红枣可溶性糖含量条件的优化[J]. 食品科学, 2014, 35(24): 136−140 doi: 10.7506/spkx1002-6630-201424026 WEI J, WU C Y, JIANG Y, et al. Sample preparation optimization for determination of soluble sugar in red jujube fruits by anthrone method[J]. Food Science, 2014, 35(24): 136−140 doi: 10.7506/spkx1002-6630-201424026
[17] 国家药典委员会. 中华人民共和国药典[S]. 一部. 北京: 中国医药科技出版社, 2020: 276–277 Chinese Pharmacopoeia Commission. Pharmacopoeia of the People’s Republic of China[S]. Beijing: China Medical Science Press, 2020: 276–277
[18] 匡双便, 徐祥增, 孟珍贵, 等. 不同透光率对三七生长特征及根皂苷含量的影响[J]. 应用与环境生物学报, 2015, 21(2): 279−286 KUANG S B, XU X Z, MENG Z G, et al. Effects of light transmittance on plant growth and root ginsenoside content of Panax notoginseng[J]. Chinese Journal of Applied and Environmental Biology, 2015, 21(2): 279−286
[19] 何忠俊, 黄希, 梁社往, 等. 滇重楼根茎皂苷含量与生态因子的关系[J]. 生态环境学报, 2016, 25(3): 409−414 HE Z J, HUANG X, LIANG S W, et al. Relationships between total saponin content in rhizome of Paris polyphylla var. yunnannensis and ecological factors[J]. Ecology and Environmental Sciences, 2016, 25(3): 409−414
[20] 吴长桥, 张睿胤, 穆德添, 等. 七叶一枝花糖基转移酶基因的克隆及表达分析[J]. 分子植物育种, 2021, 19(9): 2881−2888 WU C Q, ZHANG R Y, MU D T, et al. Cloning and expression analysis of glycosyltransferase in Paris polyphylla Smith var. chinensis (Franch.) Hara[J]. Molecular Plant Breeding, 2021, 19(9): 2881−2888
[21] LI A M, LI S H, WU X J, et al. Influence of light intensity on the yield and quality of Houttuynia cordata[J]. Plant Production Science, 2015, 18(4): 522−528 doi: 10.1626/pps.18.522
[22] 郭品湘, 尹婷, 粟春青, 等. 遮阴对双色木番茄幼苗生理特性的影响[J]. 森林与环境学报, 2020, 40(1): 76−82 GUO P X, YIN T, SU C Q, et al. Effects of shade on the physiological characteristics of Solanum wrightii seedlings[J]. Journal of Forest and Environment, 2020, 40(1): 76−82
[23] 苏文华, 张光飞, 李秀华, 等. 植物药材次生代谢产物的积累与环境的关系[J]. 中草药, 2005, 36(9): 1415−1418 doi: 10.3321/j.issn:0253-2670.2005.09.052 SU W H, ZHANG G F, LI X H, et al. Relationship between accumulation of secondary metabolism in medicinal plant and environmental condition[J]. Chinese Traditional and Herbal Drugs, 2005, 36(9): 1415−1418 doi: 10.3321/j.issn:0253-2670.2005.09.052
[24] KOUKI M, MANETAS Y. Resource availability affects differentially the levels of gallotannins and condensed tannins in Ceratonia siliqua[J]. Biochemical Systematics and Ecology, 2002, 30(7): 631−639 doi: 10.1016/S0305-1978(01)00142-9
[25] 李合生. 现代植物生理学[M]. 北京: 高等教育出版社, 2002 LI H S. Modern Plant Physiology[M]. Beijing: Higher Education Press, 2002
[26] 孙克香, 杨莎, 郭峰, 等. 高温强光胁迫下外源钙对甜椒(Capsicum fructescens L.)幼苗光合生理特性的影响[J]. 植物生理学报, 2015, 51(3): 280−286 SUN K X, YANG S, GUO F, et al. Effects of exogenous calcium on photosynthetic chracteristics of sweet pepper (Capsicum fructescens L.) seedlings[J]. Plant Physiology Journal, 2015, 51(3): 280−286
[27] 黄河腾, 黄剑坚, 陈杰, 等. 不同遮阴环境下木奶果幼苗生长与生理生化的响应[J]. 生态学杂志, 2020, 39(5): 1538−1547 HUANG H T, HUANG J J, CHEN J, et al. Growth, physiological and biochemical response of Baccaurea ramiflora Lour. seedlings to different shading environments[J]. Chinese Journal of Ecology, 2020, 39(5): 1538−1547
[28] 吴能表, 李琳琳, 杨卫星, 等. 光强对长春花叶片碳氮及次生代谢产物积累的影响[J]. 草业科学, 2014, 31(8): 1508−1514 doi: 10.11829/j.issn.1001-0629.2013-0584 WU N B, LI L L, YANG W X, et al. Effects of light intensity on carbon-nitrogen metabolism and secondary metabolite of Catharanthus roseus leaves[J]. Pratacultural Science, 2014, 31(8): 1508−1514 doi: 10.11829/j.issn.1001-0629.2013-0584
[29] 陶巧静, 吴月燕, 付涛, 等. 弱光胁迫对西洋杜鹃生理特性和叶片超微结构的影响[J]. 林业科学, 2015, 51(3): 84−92 TAO Q J, WU Y Y, FU T, et al. Effect of low light stress on physiological characteristics and ultrastructure of Rhododendron hybridum leaves[J]. Scientia Silvae Sinicae, 2015, 51(3): 84−92
[30] 徐明远, 王谦博, 郭盛磊, 等. 遮光对刺五加生长以及光合生理参数的影响[J]. 中国实验方剂学杂志, 2020, 26(20): 140−145 XU M Y, WANG Q B, GUO S L, et al. Effect of shading on growth and photosynthetic physiological parameters of Acanthopanax senticosus[J]. Chinese Journal of Experimental Traditional Medical Formulae, 2020, 26(20): 140−145
[31] 严晓芦, 郭巧生, 史红专, 等. 光照强度对紫花地丁生长、生理及化学成分的影响[J]. 中国中药杂志, 2019, 44(6): 1119−1125 YAN X L, GUO Q S, SHI H Z, et al. Effects of light intensities on growth, physiological characteristic and chemical composition of Viola yedoensis[J]. China Journal of Chinese Materia Medica, 2019, 44(6): 1119−1125
[32] 季本华, 朱素琴, 焦德茂. 不同温光条件下籼粳稻叶片的光能转化效率和膜脂过氧化表现[J]. 作物学报, 2001, 27(6): 743−750 JI B H, ZHU S Q, JIAO D M. Light energy conversion efficiency and membrane lipid peroxidation in leaves of indica and Japonica rice (Oryza sativa L.) under different temperatures and light intensities[J]. Acta Agronomica Sinica, 2001, 27(6): 743−750
[33] 吕冬煦, 倪海瑞, 曾彦达. 光照强度对水稻HS叶片失绿的影响[J]. 中国农学通报, 2020, 36(20): 23−27 LYU D X, NI H R, ZENG Y D. Light intensity: effects on leaf chlorosis of rice HS[J]. Chinese Agricultural Science Bulletin, 2020, 36(20): 23−27
-
期刊类型引用(11)
1. 刘佳,曹基武,彭翠英,王靖涵,王旭军. 土壤化学性质对七叶一枝花产量和品质的影响. 中国野生植物资源. 2025(01): 14-22 .  百度学术
百度学术
2. 刘佳,曹基武,彭翠英,王靖涵,梁军生,廖德志,王旭军. 土壤酚酸类物质对七叶一枝花农艺性状的影响. 湖南林业科技. 2024(02): 10-15+24 .  百度学术
百度学术
3. 陆奇丰,骆文华. 极小种群广西火桐幼苗对干旱复水的生理响应. 西南林业大学学报(自然科学). 2024(04): 8-16 .  百度学术
百度学术
4. 冯敬华,陈邦清,陈显,曾百林,田风雷,王功芳,余长蓉,曹荣军,张永翠,李道新. 七叶一枝花人工丰产栽培技术研究. 绿色科技. 2024(13): 70-74+78 .  百度学术
百度学术
5. 刘守赞,蒋玲苔,张韵,顾依雯,韩敏琪,李姗,王红珍,白岩. 蓝、紫单色光处理对三叶青生理及总黄酮含量时空变化的影响. 中国生态农业学报(中英文). 2023(06): 885-894 .  本站查看
本站查看
6. 周水灯,孙健,江建铭,邵将炜,邓惠敏,邵清松,王志安. 不同生育期施肥对浙贝母产量和品质的影响. 浙江农林大学学报. 2023(04): 756-764 .  百度学术
百度学术
7. 陆奇丰,骆文华. 不同遮阴环境对广西火桐幼苗生长及生理生化的影响. 西部林业科学. 2023(04): 70-76+82 .  百度学术
百度学术
8. 米琪,赵艳丽,李文春,普伟,陆尤,徐萍,于梦雯,陈佳,郑国伟. 云南重楼与球药隔重楼皂苷含量差异及光合特性研究. 时珍国医国药. 2023(12): 2937-2941 .  百度学术
百度学术
9. 陈思,阎凯,何永美,湛方栋,祖艳群,李元,陈建军,李博. 遮阴对伴矿景天Cd、Pb、Zn累积特征的影响. 中国生态农业学报(中英文). 2022(03): 409-418 .  本站查看
本站查看
10. 李坤,毛纯,刘军,吴芳兰,杨梅. LED光质对走马胎生长和生理及活性成分含量的影响. 西北植物学报. 2022(05): 819-828 .  百度学术
百度学术
11. 许涛,郝心悦,于远航,庄心情,武淑娟,张怡. “药光互补”模式下中草药种植研究概述. 低碳世界. 2022(11): 169-171 .  百度学术
百度学术
其他类型引用(4)



 下载:
下载: